Bagi pasien dengan penyakit serius, akses tepat waktu terhadap obat-obatan yang manjur adalah hal yang terpenting. Badan Obat Eropa (EMA) dibentuk untuk membantu mempercepat persetujuan obat dan memastikan produk ini aman dan efektif. Sebagaimana dinyatakan dalam makalah oleh Grünwald dan Stargardt (2024):
EMA (European Medicines Agency) didirikan pada tahun 1995 terutama untuk menyelaraskan izin edar obat-obatan di UE dan EEA…karena terdapat perbedaan besar antar negara-negara Eropa dalam hal penundaan peluncuran dan ketersediaan obat-obatan
EMA memiliki 3 prosedur komunitas utama yang memberikan akses ke pasar beberapa atau seluruh negara anggota UE secara bersamaan.
- Prosedur terpusat (CP). Jika EMA mengevaluasi suatu obat dan memberikan izin edar, keputusan ini mengikat semua negara anggota Uni Eropa. CP diperkenalkan pada tahun 1995 dan awalnya hanya digunakan untuk “proses bioteknologi, seperti antibodi monoklonal, ekspresi gen terkontrol, atau teknologi DNA rekombinan”. Daftar pengobatan yang dievaluasi berdasarkan CP telah diperluas hingga mencakup obat-obatan dan zat-zat yang tidak digunakan lagi untuk melawan kanker, diabetes, dan HIV/AIDS (pada tahun 2005), penyakit akibat virus dan penyakit/disfungsi autoimun (pada tahun 2008), dan produk obat terapi tingkat lanjut (misalnya, terapi sel dan gen) juga pada tahun 2008.
- Prosedur saling pengakuan (MRP). Dalam hal ini, penilaian dilakukan oleh negara anggota referensi, yang mana pemohon dapat memilih secara bebas dan keputusannya kemudian diadopsi oleh semua negara anggota lainnya di mana pemohon mencari akses pasar. Prosedur ini diadopsi pada tahun 2001, dan mencakup pengobatan baru di luar CP seperti obat-obatan lain dan obat generik.
- Prosedur terdesentralisasi (DCP). Diadopsi pada tahun 2005, hal ini akan memungkinkan produsen farmasi untuk mendapatkan persetujuan dari satu negara ke negara lain. Ini hanya berlaku untuk zat baru yang tidak diatur oleh CP atau MRP.
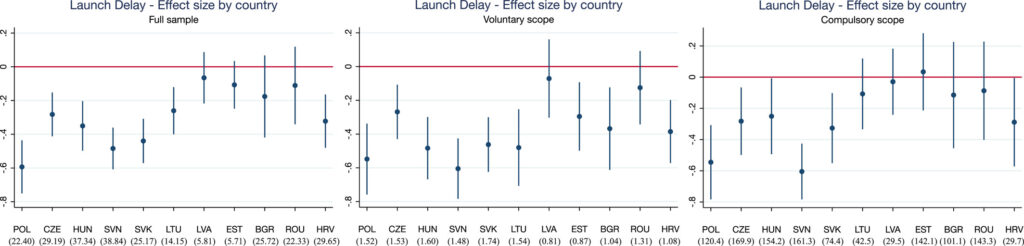
Untuk menguji dampak dari prosedur-prosedur ini, Grünwald dan Stargardt (2024) melakukan analisis perbedaan-dalam-perbedaan yang membandingkan negara-negara yang tunduk pada prosedur komunitas ini dengan negara-negara yang tidak menerapkan prosedur tersebut. Khususnya, dengan perluasan UE, pada tahun 2004 Republik Ceko, Estonia, Hongaria, Latvia, Lituania, Polandia, Slovakia dan Slovenia (Siprus dan Malta juga bergabung dengan UE pada tanggal ini namun penulis tidak memiliki data dari negara-negara tersebut). Pada tahun 2007, Bulgaria dan Rumania bergabung dengan UE dan kemudian Kroasia bergabung pada tahun 2013. Sebaliknya, Belarus, Bosnia dan Herzegovina, Kazakhstan, Rusia, Serbia, Swiss, dan Turki tidak pernah bergabung dengan UE. Dengan menggunakan data penjualan IQVIA dari 33 negara Eropa, penulis meneliti (i) penundaan peluncuran dan (ii) ketersediaan zat aktif baru. Para penulis menemukan bahwa,
…negara-negara mengalami penurunan rata-rata penundaan peluncuran sebesar 10,9 bulan (P = 0,004) setelah bergabung dengan UE. Efek yang lebih tinggi terjadi pada obat-obatan yang termasuk dalam indikasi yang mungkin secara sukarela berpartisipasi dalam CP namun tidak diwajibkan untuk berpartisipasi. Hal ini seringkali kurang menarik secara finansial bagi produsen dibandingkan dengan obat-obatan yang termasuk dalam lingkup wajib. Ketersediaan obat-obatan baru yang diluncurkan tetap tidak terpengaruh. Kami menemukan tanda-tanda bahwa besarnya dampak izin edar terpusat terhadap penundaan peluncuran di suatu negara mungkin dipengaruhi oleh keputusan strategis produsen di tingkat nasional (misalnya, perdagangan paralel atau penetapan harga referensi).
Untuk lebih jelasnya, Anda dapat membaca artikel selengkapnya Di Sini.