Ketika kita memikirkan manajemen pemanfaatan (misalnya, otorisasi sebelumnya, pengeditan langkah), kita sering berpikir pembayar hanya menggunakan ini untuk produk bermerek dengan biaya lebih tinggi termasuk produk biologis. Obat generik harus mempunyai cost sharing yang rendah dan manajemen pemanfaatan yang terbatas. Namun yang menjadi pertanyaan adalah apakah praktik manajemen pemanfaatan biosimilar yang dilakukan pembayar mencerminkan praktik produk biologis, atau obat generik bermolekul kecil, atau di antara keduanya.
Makalah oleh Yu dkk. (2023) bertujuan untuk menjawab pertanyaan ini. Para penulis menggunakan data dari database Tufts Medical Center Specialty Drug Evidence and Coverage (SPEC) yang mencakup 19 biosimilar yang tersedia secara komersial sesuai dengan 7 produk referensi. Produk-produk ini digunakan untuk 28 indikasi unik. Para penulis menemukan bahwa:
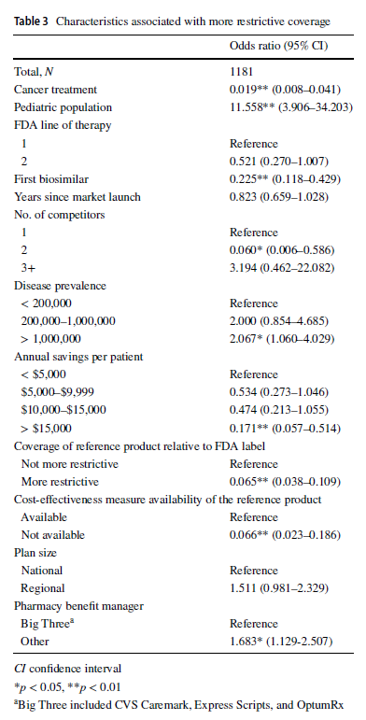
Dibandingkan dengan produk referensi, rencana kesehatan memberlakukan pengecualian cakupan atau pembatasan terapi bertahap pada biosimilar di 229 (19,4%) keputusan. Rencana tersebut lebih cenderung membatasi cakupan biosimilar untuk populasi anak (rasio odds (OR) 11.558, interval kepercayaan (CI) 95% 3.906–34.203), pada penyakit dengan prevalensi di AS lebih tinggi dari 1.000.000 (OR 2.067, 95% CI 1.060–4.029 ), dan jika rencana tersebut tidak berkontrak dengan salah satu dari tiga manajer manfaat farmasi utama (OR 1,683, 95% CI 1,129–2,507). Dibandingkan dengan produk referensi, rencana tersebut cenderung tidak memberlakukan pembatasan pada pasangan biosimilar-indikasi jika biosimilar tersebut diindikasikan untuk pengobatan kanker (OR 0,019, 95% CI 0,008–0,041), jika produk tersebut adalah biosimilar pertama (OR 0,225, 95% CI 0,118–0,429), jika biosimilar memiliki dua pesaing (termasuk produk referensi; OR 0,060, 95% CI 0,006–0,586), jika biosimilar dapat menghasilkan penghematan harga tahunan lebih dari $15.000 per pasien (OR 0,171, 95 % CI 0,057–0,514), jika produk referensi biosimilar dibatasi oleh rencana (OR 0,065, 95% CI 0,038–0,109), atau jika ukuran efektivitas biaya tidak tersedia (OR 0,066, 95% CI 0,023–0,186) .
Salah satu temuan menarik adalah bahwa PBM berukuran besar sebenarnya memiliki kebijakan yang tidak terlalu ketat terhadap biosimilar. Mengapa?
… Ada anggapan bahwa daya tawar PBM yang lebih besar mungkin begitu signifikan sehingga produsen biosimilar terkadang menaikkan harga jual, dan dengan demikian rabat, untuk mendapatkan tempat di formularium PBM yang besar. Hal ini akan menyebabkan PBM yang lebih kecil memiliki harga jual yang lebih tinggi
potongan harga yang lebih kecil karena daya tawarnya yang relatif lebih kecil, sehingga biosimilar memberikan nilai yang lebih kecil bagi mereka.
Anda dapat membaca makalah selengkapnya Di Sini.